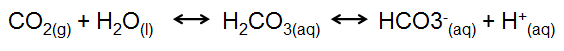如果做個問卷調查「常吃肉會造成酸性體質?」,應該有不少人會說對,先來看一則對岸的科普節目《原來如此》
很精彩的一集!其中提及人體血液是一種生理緩衝溶液(buffer solution),在中學提到緩衝溶液時,通常老師會先做個實驗來示範這種緩衝作用:
影片左方燒杯中的水只要加入1滴1M的鹽酸,其pH值立刻由7變為2;但是在右邊的緩衝溶液中則必須加入85滴1M的鹽酸,其pH值才能由7變為2。接著在左方燒杯中的水加入2滴1M的鹼性氫氧化鈉溶液,其pH值由2變為10;同樣的在右邊的緩衝溶液中必須加入約200滴1M的氫氧化鈉溶液,其pH值才能由2變為10。做完這個示範實驗後,老師就會講解在緩衝溶液中無論加入酸、鹼或是稀釋時,為什麼pH值不會發生大幅度變化的原因。
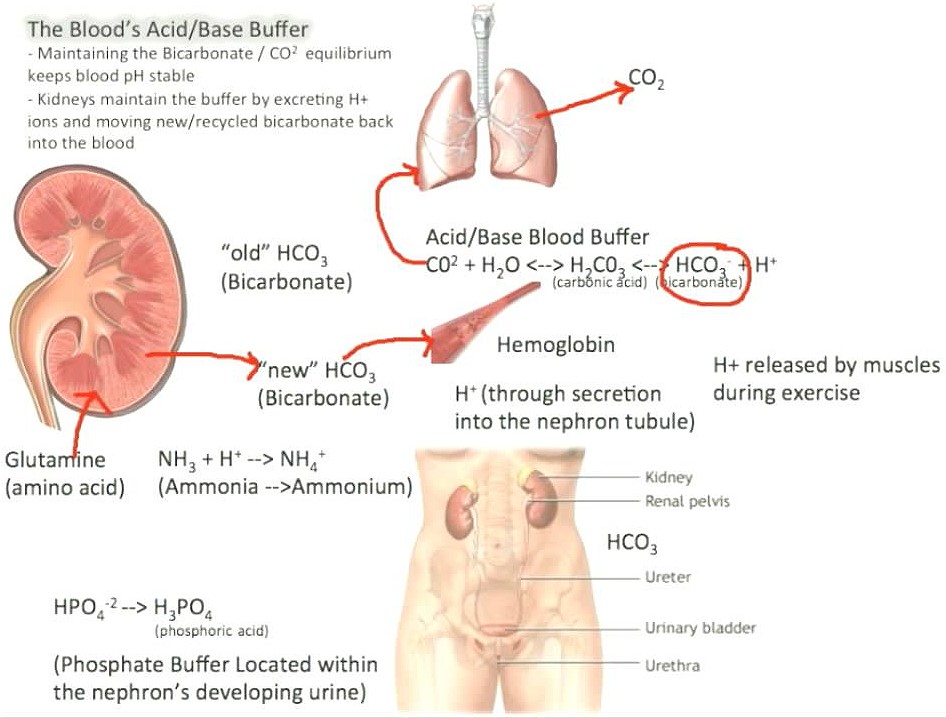
至於 人體血液的緩衝作用,是藉由溶解在血液中的緩衝劑來達成,加上肺與腎等器官的協助來提高緩衝劑的效能。其中肺臟提供較為快速的方法以控制血液中的pH值,譬如運動時增加呼吸速率即能移走二氧化碳,幫助抵消運動時酸鹼度降低的影響(呼吸性酸中毒即是肇因於肺臟無法即時消除所產生的二氧化碳);至於腎則是幫忙移走血液中過量的HCO3–來幫助降低pH值,不過這種經由腎臟的排泄作用相對較為緩慢。
以運動而言,當肌肉將葡萄糖的化學能轉變為機械能時,需要利用血液中由血紅素所攜帶的氧,將葡萄糖分解產生二氧化碳和氫離子(H+),並將其從肌肉移出至血液中。因此除非能藉著其他生理功能的彌補,否則二氧化碳和氫離子將導致血液 pH值降低。血液的正常pH值應維持在 7.4,如果 pH值小於6.8就有可能造成死亡。至於血液pH值的調節,主要是依賴其中的H2CO3/HCO3–緩衝溶液系統來達成,透過此系統能緩衝運動所產生的酸或者大量飲水所造成體液的稀釋狀態,使血液pH值得以維持正常。其機制是因為運動所增加的H+數量相較於血液中HCO3– 的數量少很多,因此這些H+就能經由與HCO3– 結合成H2CO3來達到減緩H+的變化。再加上肺臟能移走來自血液中過量的CO2 (運動直接產生的CO2 、H+與HCO3– 結合成H2CO3然後分解生成的CO2),血液因而能維持 pH值 7.4 的恆定狀態。同理,當人體吃進肉類與碳水化合物等食物後,在經過消化吸收代謝等作用所產生的酸性物質也是經由相同的模式從肺臟將生成的CO2排出體外,血液pH值仍然是維持在 7.4的最佳狀態。反之,當食物代謝後呈現鹼性的狀況(例如影片中檸檬燃燒後所產生的鹽類),則是藉由腎臟移走體內過量的HCO3–來幫助降低pH值。勒沙特列原理可用來解釋腎臟如何幫助預防過高的pH值(即鹼中毒的情況)。
當腎臟減少血液中HCO3–的濃度後,根據勒沙特列原理,上式的平衡反應會向右移動以彌補失去的HCO3–。當平衡向右移動,更多的H+ 離子和HCO3–便會一起產生,pH值於是降低,所以最後還是能達到血液pH值的恆定。學校的老師講到這裡通常會舉這個例子:若遇到過度換氣這種非常迅速且深沉的呼吸,將會導致血液中二氧化碳的濃度下降因而引起呼吸性鹼中毒(頭昏眼花),此時急救藥物就是一個紙袋,讓患者反覆吸進自己吹進紙袋裡的空氣(請思考這種紙袋治療對血液中的pH值有何影響)。不過這種治療有導致缺氧的危險,目前已經不再推薦使用,改成腹式呼吸這種能放鬆減壓的方式。
在調節血液的pH值上,除了前述的H2CO3/HCO3– ,人體還有其他濃度較低的次要緩衝物,例如磷酸鹽緩衝物(包含磷酸H3PO4和磷酸二氫根離子H2PO4– ),甚至血紅素在血液中同樣也能達成pH的緩衝作用,請見:血紅素蛋白質 。
結論:常吃肉不會造成酸性體質(不過高動物性蛋白質與高脂食物卻會增加血膽固醇)